DOI: 10.1111/eci.13998
Zależne od partii bezpieczeństwo szczepionki BNT162b2 mRNA COVID-19
Maks Schmeling 1 | Vibeke Manniche 2 | Peter Riis Hansen 3
1 Inometric, Skørping, Dania
2 LIVA, Kopenhaga, Dania
3 Katedra Kardiologii, Kobenhavns Universitet, Kopenhaga, Dania
Korespondencja
Peter Riis Hansen, Wydział Kardiologii, Kobenhavns Universitet, Kopenhaga, Dania. E-mail: prha@sund.ku.dk
Do Redakcji ,
Szczepienia zostały szeroko wdrożone w celu złagodzenia choroby koronawirusowej 2019 (Covid-19), a do 11 listopada 2022 r. podano 701 milionów dawek szczepionki mRNA BNT162b2 (Pfizer-BioNTech), co powiązano z 971 021 doniesieniami o podejrzewanych działaniach niepożądanych ( SAE) w Unii Europejskiej/Europejski Obszar Gospodarczy (UE/EOG). 1 Fiolki ze szczepionką z indywidualnymi dawkami są dostarczane w partiach z rygorystyczną kontrolą jakości, aby zapewnić jednolitość serii i dawek. 2 Nie przedstawiono danych klinicznych dotyczących poszczególnych poziomów serii szczepionek, a zależne od partii różnice w skuteczności klinicznej i bezpieczeństwie szczepionek dopuszczonych do obrotu wydają się wysoce nieprawdopodobne. Jednakże, nie tylko ze względu na dopuszczenie do obrotu do użytku w sytuacjach awaryjnych i szybkie wdrożenie programów szczepień na dużą skalę, możliwość zmienności zależnej od serii wydaje się warta zbadania. Dlatego zbadaliśmy wskaźniki SAE między różnymi partiami szczepionki BNT162b2 podanymi w Danii (populacja 5,8 miliona) od 27 grudnia 2020 r. do 11 stycznia 2022 r.
Dane dotyczące wszystkich przypadków SAE z odpowiednimi etykietami serii szczepionek zgłoszonych do Duńskiej Agencji Medycznej (DKMA) i sklasyfikowanych przez DKMA zgodnie z ciężkością SAE oraz liczby dawek BNT162b2 w poszczególnych seriach szczepionek zarejestrowanych odpowiednio przez Duński Instytut Serum są publicznie dostępne i zostały odzyskane na żądanie. Zarządzany przez DKMA system spontanicznego zgłaszania SAE przyjmuje zgłoszenia SAE z dowolnego źródła, na przykład od dostawców opieki zdrowotnej, pacjentów i innych członków społeczeństwa. Do SAE przypisano terminy ze słownika medycznego dla czynności regulacyjnych (MedDRA), które niekoniecznie odpowiadają zweryfikowanym diagnozom medycznym, a do raportu można przypisać więcej niż 1 SAE. Stopień ciężkości SAE klasyfikowano odpowiednio jako nieciężki, ciężki (hospitalizacja lub przedłużenie istniejącej hospitalizacji, choroba zagrażająca życiu, trwałe kalectwo lub wrodzona wada rozwojowa) lub zgon związany z SAE. Badanie opierało się wyłącznie na wtórnym wykorzystaniu tych zanonimizowanych danych i dlatego było zwolnione z przeglądu komisji ds. etyki badań. SAE zliczono na poziomie partii przez powiązanie poszczególnych SAE z etykietą(ami) partii dawki(ów) BNT162b, którą otrzymał osobnik. Całkowitą liczbę SAE związanych z każdą partią podzielono przez liczbę dawek w partii, aby uzyskać wskaźnik SAE na 1000 dawek. Ponieważ obserwowany związek między liczbą SAE a dawkami szczepionki BNT162b2 był wysoce niejednorodny, uznano, że konwencjonalne statystyki regresji nie mają zastosowania. W związku z tym heterogeniczność zależności między liczbą SAE a dawkami przypadającymi na partię szczepionki oceniono za pomocą transformacji logarytmicznej, a następnie niehierarchicznej analizy skupień i testu ogólnego modelu liniowego (GLM) pod kątem różnic we wskaźnikach SAE między partiami. Raportowanie z badania jest zgodne z ogólnymi wytycznymi EQUATOR. 3 [Poprawka dodana 13 kwietnia 2023 r., po pierwszej publikacji online: w tej wersji zaktualizowano afiliację odpowiedniego autora]
Jest to artykuł o otwartym dostępie na warunkach licencji Creative Commons Attribution-NonCommercial License, która zezwala na używanie, dystrybucję i powielanie na dowolnym nośniku, pod warunkiem, że oryginalne dzieło jest odpowiednio cytowane i nie jest wykorzystywane w celach komercyjnych.
© 2023 Autorzy. European Journal of Clinical Investigation opublikowane przez John Wiley & Sons Ltd w imieniu Stichting European Society for Clinical Investigation Journal Foundation.
Eur J Clin Invest. 2023;00:e13998. wileyonlinelibrary.com/journal/eci | 1 z 3 https://doi.org/10.1111/eci.13998
Łącznie podano 10 793 766 dawek 4 026 575 osobom przy użyciu 52 różnych partii szczepionki BNT162b2 (2340– 814 320 dawek na serię) i zarejestrowano 43 496 SAE u 13 635 osób, co odpowiada 3,19 ± 0,03 (średnia ± SEM) SAE na osobę . [Poprawka dodana 9 czerwca 2023 r., po pierwszej publikacji online: W poprzednim oświadczeniu poprawiono łączną liczbę dawek i liczbę pacjentów]. U każdej osoby poszczególne SAE były związane z dawkami szczepionki z 1,531 ± 0,004 partii, co dało w sumie 66 587 SAE rozdzielonych między 52 partie. W przypadku 7,11% SAE etykiety serii były niekompletnie zarejestrowane lub ich brak, pozostawiając 61 847 SAE możliwych do zidentyfikowania w serii, z których 14 509 (23,5%) sklasyfikowano jako ciężkie SAE, a 579 (0,9%) stanowiły zgony związane z SAE. Nieoczekiwanie częstość SAE na 1000 dawek różniła się znacznie pomiędzy seriami szczepionek i wynosiła 2,32 (0,09–3,59) (mediana [przedział międzykwartylowy]) SAE na 1000 dawek, a także zaobserwowano istotną heterogeniczność ( p < 0,0001) w zależności między liczbami SAE na 1000 dawek i liczby dawek w poszczególnych seriach. Wyróżniono trzy dominujące linie trendu, z zauważalnymi niższymi wskaźnikami SAE w większych partiach szczepionek i dodatkową heterogenicznością zależną od serii w rozkładzie ciężkości SAE między seriami reprezentującymi trzy linie trendu ( Ryc . 1 ).
W porównaniu ze wskaźnikami wszystkich SAE, poważne SAE i zgony związane z SAE na 1000 dawek były znacznie rzadsze, a liczba tych SAE na 1000 dawek wykazywała znacznie większą zmienność między partiami, z mniejszą separacją między trzema liniami trendu (nie pokazano).
Zaobserwowane zróżnicowanie częstości SAE i nasilenia SAE między partiami szczepionki BTN162b2 w tym ogólnokrajowym badaniu było sprzeczne z oczekiwaną jednorodną częstością i rozkładem SAE między seriami. W Danii i innych krajach UE/EOG jakość szczepionek jest monitorowana zgodnie z wytycznymi oficjalnego organu kontrolnego ds. zwalniania serii (OCABR) i według naszej wiedzy potencjalne różnice w bezpieczeństwie klinicznym lub skuteczności serii szczepionki BNT162b2 nie były wcześniej zgłaszane, na przykład próby autoryzacyjne i późniejsze badania populacyjne. 4,5 Takie skutki mogą być łatwiejsze do wykrycia w małych krajach, takich jak Dania, gdzie szczepionki BNT162b2 w okresie badania były na ogół dostarczane w kilku mniejszych partiach. Ponadto monitorowanie regulacyjne i zainteresowanie naukowe bezpieczeństwem szczepionek przeciwko COVID-19 koncentrowały się przede wszystkim na poważnych zdarzeniach niepożądanych, takich jak zapalenie mięśnia sercowego. 6 W każdym przypadku identyfikacja takich skutków oczywiście wymaga powiązania zaobserwowanych zdarzeń niepożądanych z odpowiednimi etykietami poszczególnych serii i wielkością (numerami dawek). Wcześniej zmienność w
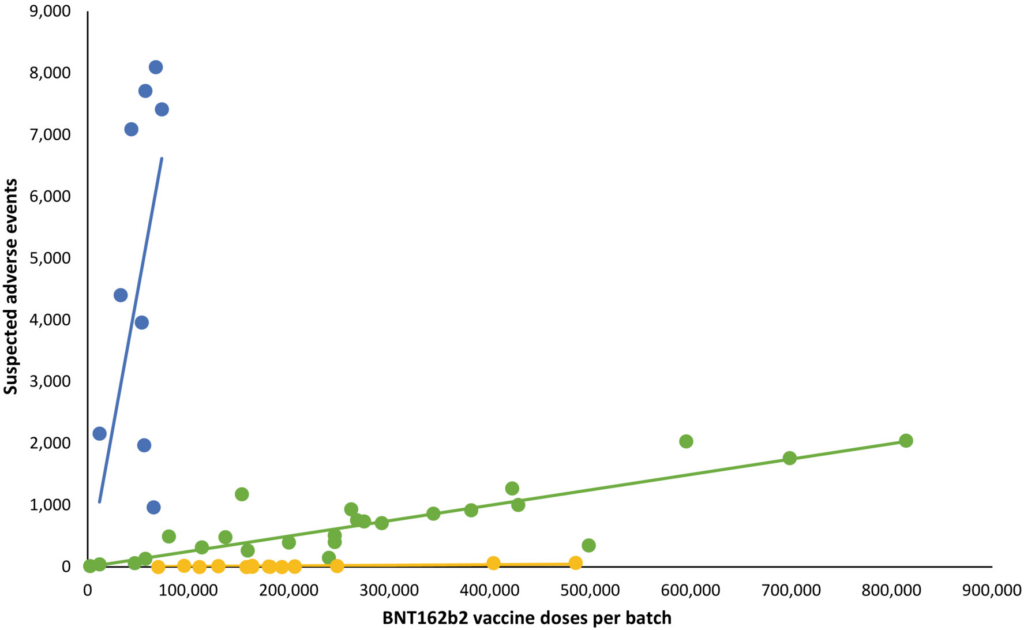
WYKRES 1 Liczba podejrzewanych zdarzeń niepożądanych (SAE) po szczepieniu mRNA BNT612b2 w Danii (27 grudnia 2020 r. – 1 stycznia 2022 r.) według liczby dawek na partię szczepionki. Każda kropka reprezentuje pojedynczą partię szczepionki. Linie trendu to linie regresji liniowej. Niebieski: R2 = 0,78, β = 0,0898 (95% przedział ufności [CI] 0,0514–0,1281), zielony: R2 = 0,89 , β = 0,0025 (95% CI 0,0021–0,0029), żółty: R2 = 0,68, β = 0,000087 (95% przedział ufności 0,000056–0,000118). Partie szczepionek reprezentujące niebieską, zieloną i żółtą linię trendu stanowiły odpowiednio 4,22%, 63,69% i 32,09% wszystkich dawek szczepionki, z 70,78%, 27,49% i 47,15% (niebieska linia trendu), 28,84%, 71,50% i 51,99% (zielona linia linia trendu) oraz 0,38%, 1,01% i 0,86% (żółta linia trendu) odpowiednio wszystkich SAE, poważnych SAE i zgonów związanych z SAE.
Wykazano, że produkcja (wzrost hodowli) szczepionki Bacille Calmette-Guérin wpływa na ważne efekty immunologiczne tej szczepionki, 7 i dwa przypadki zapalenia mięśnia sercowego zostały zgłoszone u dwóch młodych mężczyzn po otrzymaniu szczepionki mRNA-1 273 COVID- 19 (Moderna) z tej samej partii szczepionki tego samego dnia. 8 Rzeczywiście, zmiany (z partii na partię, z fiolki na fiolkę, a nawet z dawki na dawkę) w szczepionkach mogą wystąpić w wyniku zmienności i naruszeń w praktyce, na przykład w produkcji szczepionek, przechowywaniu, transporcie, postępowaniu klinicznym i kontrolnych, aw 2021 r. w Japonii wycofano trzy serie szczepionki mRNA1273 o łącznej wartości ponad 1,6 miliona dawek po tym, jak stwierdzono, że 39 fiolek szczepionki zawiera obce materiały. 9 Wyciekłe i zakwestionowane dane sugerują również, że niektóre wczesne komercyjne partie szczepionki BNT162b2 zawierały niższe niż oczekiwano poziomy nienaruszonego mRNA. 10
Obecne wstępne ustalenia należy interpretować w świetle kilku ograniczeń. Zarządzany przez DKMA system spontanicznego zgłaszania SAE w Danii jest pasywnym systemem nadzoru, podobnym do systemu zgłaszania zdarzeń niepożądanych poszczepiennych (VAERS) w USA, a zgłoszenia z tych systemów podlegają błędom sprawozdawczym, z możliwością zarówno niedoszacowania, jak i zawyżenia raportowania, a także niepełne dane i zróżnicowana jakość przekazywanych informacji. 11,12 Ze względu na te nieodłączne ograniczenia sygnały wykrywane przez te systemy muszą być uważane za generujące hipotezy i generalnie nie mogą być wykorzystywane do ustalenia związku przyczynowego. 11-14 Ponadto w niniejszym badaniu historia przypadków SAE wcześniejszego COVID-19 była nieznana, a określone typy SAE (klasa układów i narządów MedDRA itp.), dane demograficzne przypadków SAE, związki SAE z kolejnymi dawkami szczepionki u poszczególnych osób przypadków, nie zbadano trendów czasowych obserwowanej zależności SAE od serii i zależnego od serii wpływu na skuteczność szczepionki. Warto zauważyć, że według naszej wiedzy Duński Instytut Serum nie wycofał serii szczepionek BNT162b2. Podsumowując, wyniki sugerują istnienie zależnego od serii sygnału bezpieczeństwa dla szczepionki BNT162b2 i uzasadnione są dalsze badania w celu zbadania tej wstępnej obserwacji i jej konsekwencji.
OŚWIADCZENIE O KONFLIKCIE INTERESÓW
Nic.
ORCID
Peter Riis Hansen https://orcid.org/0000-0002-9056-535X BIBLIOGRAFIA
źródło: https://world-scam.com/Files/Eur%20J%20Clin%20Investigation%20-%202023%20-%20Schmeling%20-%20Batch%E2%80%90dependent%20safety%20of%20the%20BNT162b2%20mRNA%20COVID%E2%80%9019%20vaccine_pl.pdf
